Публикация компании «Инвестиционная Корпорация»
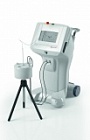
Все медицинские изделия (МИ), предназначенные для использования на российском рынке, в обязательном порядке должны проходить процедуру государственной регистрации и сертификации (декларирования). Это позволяет исключить возможность продажи и использования некачественных и неэффективных изделий. Росздравнадзор, контролирующий оборот МИ в России, производит регистрацию на основании результатов испытаний и экспертиз. Крупных испытательных центров, оказывающих высокопрофессиональные услуги производителям и продавцам медицинской техники, на рынке не более 15. В число лидеров входит Центр испытаний и сертификации продукции «ИНКОР», созданный в 2003 г. с целью оказания сертификационных услуг в сфере производства изделий медицинского назначения и электрооборудования. О деятельности центра рассказывает один из его создателей Геннадий Волков.
Геннадий, какие услуги оказывает центр в области подтверждения соответствия МИ требованиям нормативных документов, действующих на территории РФ?
Центр проводит все виды испытаний, необходимых для получения сертификата и регистрационного удостоверения, без которых невозможны ввоз, продажа и использование медтехники в России. Федеральной службой по аккредитации и Росздравнадзором мы уполномочены на проведение сертификационных, приемочных, периодических, квалификационных, ресурсных, типовых и технических испытаний.
Во время проведения испытаний мы не только проверяем безопасность медицинского оборудования, но и доказываем качество и эффективность МИ.
Сердцем любого испытательного центра можно считать его лабораторию…
Пожалуй, так. Полезная площадь нашей лаборатории — более 700 кв. м. Здесь размещаются уникальное испытательное оборудование и изделия, подвергаемые испытаниям. Большая площадь — одно из наших преимуществ, ведь для некоторых лабораторий вопрос габаритов изделия становится решающим в принятии решения о возможности проведения его испытаний.
 Лаборатория оснащена всеми необходимыми средствами измерения, новейшим испытательным оборудованием и документированными процедурами,
Лаборатория оснащена всеми необходимыми средствами измерения, новейшим испытательным оборудованием и документированными процедурами,
Метрологическая служба лаборатории постоянно проводит мониторинг испытательного оборудования (ИО) и средств измерений (СИ) на соответствие требованиям вновь изданных стандартов, при необходимости модернизируя и закупая новые ИО и СИ. Действующие ИО и СИ проходят периодическую аттестацию, поверку и калибровку.
В результате испытаний и измерений выносятся критичные решения, поэтому задачу подтверждения метрологических характеристик мы доверяем только проверенным и надежным организациям: государственным институтам ЦСМ, ВНИИМС, ВНИИФТРИ и др.
Наш высококвалифицированный персонал обладает большим стажем и практическим опытом работы в области сертификации/декларирования и испытаний продукции. Сотрудники лаборатории ежегодно проходят курсы повышения квалификации, участвуют в семинарах и конференциях, организованных Росздравнадзором РФ, ВНИИИМТ, Федеральной службой по аккредитации.
Кто является вашими клиентами? Есть ли медицинские изделия, с которыми вы не работаете?
Мы принимаем на испытания практически весь спектр МИ, начиная от бинтов и резиновых перчаток и заканчивая электронным медицинским оборудованием и его программным обеспечением. Не беремся лишь за медицинские изделия
 На постоянной основе с нами работают 60 производителей и дистрибьюторов МИ. С началом кризиса количество западных заказчиков уменьшилось, а отечественных — увеличилось. Однако в августе мы вновь ощутили приток западных компаний. Их среди наших клиентов всегда было много. Дело в том, что наша лаборатория сотрудничает с несколькими нотифицированными европейскими органами, которые по результатам проведения у нас аудита признают наши протоколы испытаний на уровне европейских. Но у нас эта услуга стоит существенно дешевле, чем в Европе. По результатам этих испытаний европейские органы выдают сертификат СЕ. Заказывают СЕ и российские производители, планирующие поставлять свои изделия за рубеж.
На постоянной основе с нами работают 60 производителей и дистрибьюторов МИ. С началом кризиса количество западных заказчиков уменьшилось, а отечественных — увеличилось. Однако в августе мы вновь ощутили приток западных компаний. Их среди наших клиентов всегда было много. Дело в том, что наша лаборатория сотрудничает с несколькими нотифицированными европейскими органами, которые по результатам проведения у нас аудита признают наши протоколы испытаний на уровне европейских. Но у нас эта услуга стоит существенно дешевле, чем в Европе. По результатам этих испытаний европейские органы выдают сертификат СЕ. Заказывают СЕ и российские производители, планирующие поставлять свои изделия за рубеж.
Каким образом строится работа по сертификации СЕ?
Испытания в целях подтверждения соответствия МИ требованиям европейских директив (
На моей памяти всего
Что представляет собой процесс подтверждения соответствия?
 Он носит многоступенчатый характер и включает в себя технические испытания изделия, в том числе испытания по ЭМС, по результатам которых выдается положительный либо отрицательный протокол; токсикологические исследования; клинический протокол, необходимый для получения заключения о лечебном эффекте.
Он носит многоступенчатый характер и включает в себя технические испытания изделия, в том числе испытания по ЭМС, по результатам которых выдается положительный либо отрицательный протокол; токсикологические исследования; клинический протокол, необходимый для получения заключения о лечебном эффекте.
По итогам испытаний наши специалисты готовят пакет документов для предоставления на регистрацию в соответствующий орган сертификации — Росздравнадзор или Европейский нотифицированный орган по сертификации. Затем заказчик получает сертификат соответствия продукции национальным и международным нормам,
Наше преимущество перед большинством испытательных центров в том, что мы оказываем услуги в режиме «одного окна»
— можем взять на себя подготовку абсолютно всей разрешительной документации, которая понадобятся в процессе сертификации и регистрации МИ.
В 2012 г. вступило в силу постановление правительства РФ № 1416, регламентирующее процедуру получения регистрационного удостоверения. Но от этого она не стала проще…
Заявитель — производитель медицинского изделия либо его доверенное лицо — должен собрать комплект документов, описывающих качество, функциональность и безопасность МИ. Дело в том, что правильно и в полном объеме собрать это «регистрационное досье» довольно сложно. А оно будет подвергнуто двухэтапной экспертной оценке. Положительный результат экспертизы гарантирован, только если вся документация полностью соответствует нормативным требованиям. Даже малейшее несовпадение в документах дает основания для отрицательного результата. На первом этапе экспертной оценки осуществляется экспертиза заявления о регистрации и документов, полноты и результатов проведенных технических испытаний, токсикологических исследований, определяется возможность (невозможность) проведения клинических испытаний МИ. На втором этапе — экспертиза полноты и результатов проведенных клинических испытаний.
 Наши специалисты полностью берут на себя подготовку «медицинского досье» — от проверки правильности написанного заявления на регистрацию, оценки полноты и правильности документов до оформления протоколов технических, токсикологических и клинических испытаний и получения регистрационного удостоверения.
Наши специалисты полностью берут на себя подготовку «медицинского досье» — от проверки правильности написанного заявления на регистрацию, оценки полноты и правильности документов до оформления протоколов технических, токсикологических и клинических испытаний и получения регистрационного удостоверения.
Какие консультационные услуги оказывает ваш центр?
В рамках отдельного договора мы консультируем клиентов в области толкования и разъяснения требований законов и постановлений, других нормативных документов, стандартов, на которые, согласно требованиям Минздрава, необходимо испытывать то или иное медицинское изделие. Предоставляем нашим клиентам максимум актуальной информации, касающейся разработки нормативной документации для каждого конкретного изделия, корректируем техническую и эксплуатационную документацию. Оказываем квалифицированную помощь по написанию и корректировке технической и эксплуатационной документации на вновь разрабатываемые изделия в соответствии с требованиями ЕСКД. Разрабатываем технические условия в соответствии с
Компетентность и независимость — два ключевых качества, которыми должна обладать испытательная лаборатория. Она не имеет права давать советы производителю?
Да, по идее независимая лаборатория не должна советовать производителю, как улучшить изделие и исправить недоработки, на то она и независимая. Однако кто лучше, чем испытатель, разбирается в причине неполадок устройства? И почему бы не помочь отечественному производителю? Поэтому
по итогам проведения испытаний наши инженеры могут объяснить разработчикам, почему их МИ не соответствует требованиям стандартов РФ, а также предложить варианты конструктивного исполнения, способные обеспечить соответствие изделия заявленным характеристикам и наделить его конкурентными преимуществами.
Обычно же лаборатории вручают производителю положительный либо отрицательный протокол, предлагая ему самостоятельно разобраться, почему выходные характеристики изделия отличаются либо от заявленных в технической документации, либо от нормативных требований.
Приобретаете ли вы для лаборатории оборудование российского производства?
 Мы бы очень хотели, но далеко не все из того, что нам нужно, в России производится и выдерживает конкуренцию с западным оборудованием. Нередко, чтобы сэкономить, мы сами изготавливаем испытательное оборудование: разрабатываем конструкторскую документацию, заказываем детали, самостоятельно его собираем, пишем методики работы на нем.
Мы бы очень хотели, но далеко не все из того, что нам нужно, в России производится и выдерживает конкуренцию с западным оборудованием. Нередко, чтобы сэкономить, мы сами изготавливаем испытательное оборудование: разрабатываем конструкторскую документацию, заказываем детали, самостоятельно его собираем, пишем методики работы на нем.
Хочу отметить, что в настоящее время мы ведем строительство современной безэховой камеры электромагнитной совместимости в г. Сергиев Посад. Каркас уже готов, дело за «начинкой» — антиотражающими покрытиями, спектроанализаторами, антеннами.
Что тормозит развитие вашего сегмента рынка?
Наличие недобросовестных испытательных лабораторий. Они имеют аттестат, но не имеют ни оборудования, ни персонала, не проводят испытания и при этом выдают сертификаты. Помимо того, что они увеличивают опасность вывода на рынок некачественных изделий, они еще и занижают стоимость услуг, что сказывается на нас. Ведь качественные испытания — дело очень затратное, требующее содержания штата специалистов, модернизацию и обслуживание оборудования, выезды в командировки и др. Эти затраты могут окупиться, только если мы будем проводить испытания по их реальной стоимости. После того как на смену Госстандарту пришла Росаккредитация, контроль за аккредитованными лабораториями стал жестче, повысились требования к претендентам на аккредитацию. Тем не менее «номинальные» лаборатории умудряются обходить закон.
В скором времени Росаккредитация планирует запустить проект «сличительные межлабораторные испытания»: во время проверки лаборатории будут получать на испытания контрольные образцы техники, результат испытаний которых уже известен. Возможно, тогда выявлять недобросовестных участников рынка станет легче.
С какими еще проблемами сталкиваетесь в работе?
Несмотря на стремление российской власти к признанию общемировых правил и норм, мы отстаем от общемировой стандартизации: например, в Европе стандарт есть, а в РФ его еще нет. При этом 99% действующих в РФ стандартов — это переведенные и адаптированные стандарты, разработанные международными организациям МЭК и ИСО. Как правило, ГОСТ на основе международного стандарта актуализируется в России с запозданием в несколько лет, что мешает российскому производителю, планирующему поставлять продукцию за рубеж. Мы бы хотели приложить свои усилия в направлении разработки стандартов, однако попасть в число организаций, которые занимаются этим, нам, к сожалению, пока не удалось.
Современная база национальных стандартов несовершенна и скудна, и даже вновь выпускаемые ГОСТы зачастую не содержат всех основных требований к МИ. Поэтому совместно с разработчиками МИ мы придумываем свои, индивидуальные методики испытаний. Благо медицина — та область, в которой испытатель наделяется довольно широкими полномочиями и помимо применения стандартов вправе потребовать исполнения собственных, дополнительных требований, увеличивающих гарантии безопасности изделия.